NF-κB信号通路是调节细胞免疫应答与炎症反应、细胞存活与增殖的核心通路之一。NF-κB家族由多个成员组成,包括p50、p52、p65(RelA)、RelB和c-Rel等。这些成员通过形成同源或异源二聚体发挥功能:结合到靶基因启动子区域的κB位点,调控基因表达,其中p50/p65异源二聚体是最常见且研究最广泛的组合形式。NF-κB通路的发现距今已有近40年历史,在此期间围绕该通路开发了一系列小分子抑制剂,它们为探究NF-κB通路的生物学功能、研究该靶点相关疾病的机理作出了重大贡献。
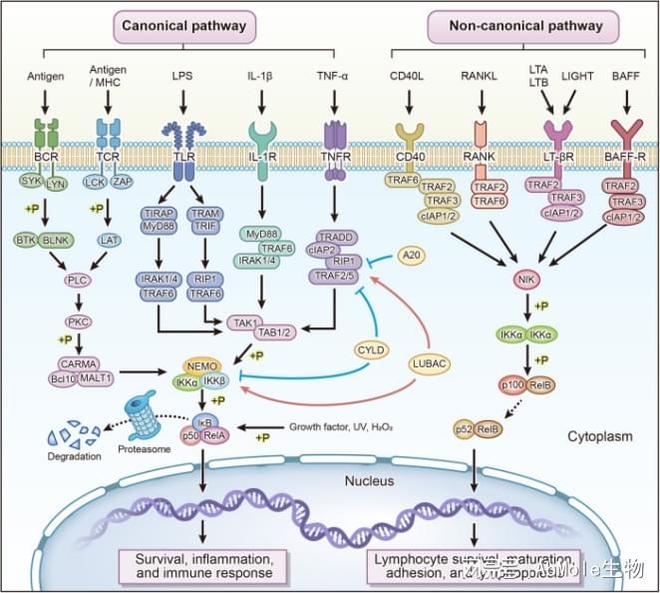
BAY 11-7082(NF-κB inhibitor 13,AbMole,南宫28M2040)是一种经典的NF-κB通路抑制剂,主要通过阻断IκB激酶(IKKβ)的活性,从而阻止IκBα的磷酸化和降解,最终抑制NF-κB p65亚基的核转位。BAY 11-7082还是一种泛素化系统的抑制剂,可通过抑制E2连接酶(如Ubc13和UbcH7)和E3泛素连接酶(如LUBAC)来阻止线炎症小体的组装及其下游效应分子(如caspase-1、IL-1β和IL-18)的释放[3]。BAY 11-7082具有显著的抗炎活性,大鼠实验显示,BAY 11-7082可缓解实验性自身免疫性神经炎(EAN)的症状,其机制涉及降低M1型巨噬细胞的比例和促炎细胞因子表达[4]。在银屑病样皮炎小鼠模型中,BAY 11-7082(CAS No.:19542-67-7)通过同时抑制NF-κB和NLRP3炎症小体,显著改善皮肤炎症[5]。此外,BAY 11-7082(BAY 11-7821)在高脂饮食诱导的代谢紊乱小鼠中,能降低肝脏和肾脏中NLRP3、caspase-1及IL-1β的水平[6]。BAY 11-7082还可诱导肿瘤细胞的凋亡,例如诱导多药耐药白血病T细胞系的凋亡[7]。
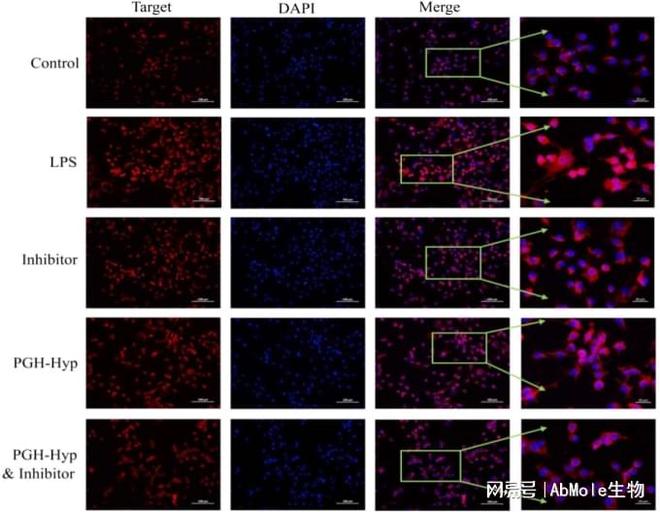
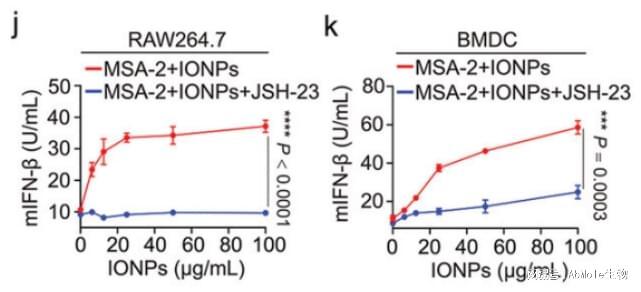
JSH-23(AbMole,M2786)是一种核因子κB(NF-κB)通路的抑制剂,IC50为 7.1 μM,与BAY 11-7082类似,也通过靶向NF-κB p65亚基的核转位发挥调控作用。JSH-23可通过抑制NF-κB信号通路的激活,从而下调促炎因子(如IL-6、TNF-α)的表达。JSH-23在LPS(Lipopolysaccharides,脂多糖)诱导的脓毒症模型小鼠中,JSH-23(3 mg/kg)通过抑制NF-κB通路减轻了心脏损伤,并减少了M1型巨噬细胞极化[9]。JSH-23(CAS No.:749886-87-1)在SD大鼠骨质疏松模型中通过TRAF6/Rac1/NOX1通路抑制破骨细胞分化,同时增强成骨细胞的Nrf2/HO-1表达以维持骨稳态[10]。JSH-23也具有抗肿瘤活性,它可抑制MDA-MB-468三阴性乳腺癌细胞的增殖与迁移,并在HepG2肝癌细胞中通过诱导G2/M期阻滞抑制细胞生长。JSH-23在阿尔茨海默病相关研究中,可恢复Aβ肽注射后的大鼠海马CA1锥体神经元的电生理特性,逆转异常增强的Ih电流[11]。这些研究共同表明,JSH-23作为NF-κB通路的工具分子,在炎症调控、肿瘤干预、神经保护及骨代谢研究中具有重要价值。
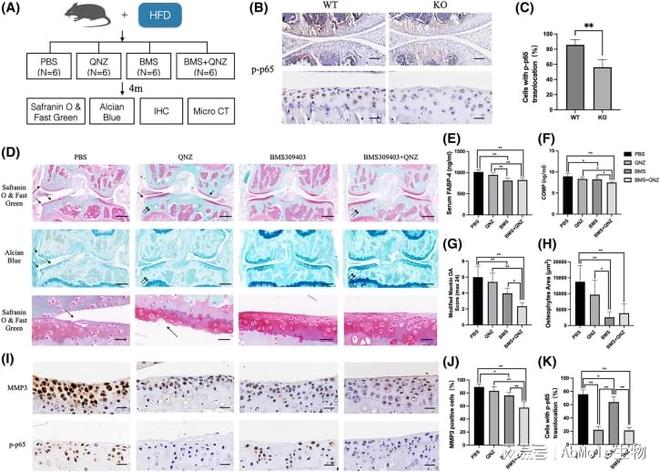
QNZ(EVP4593,AbMole,M2298)是一种NF-κB抑制剂,可抑制 NF-κB 的转录调节活性(IC50为11 nM),QNZ通过靶向抑制p65蛋白(RelA亚基)发挥调控作用。EVP4593可在大鼠肺组织中抑制TLR4/MyD88/NF-κB信号通路,进而调控肺部的炎症反应。此外,EVP4593还是一种能够抑制Orai(钙释放激活钙通道)和TRPC(经典瞬时受体电位离子通道)的化合物,同时对SOCs(内源性储存操作钙通道)也表现出抑制作用[13]。QNZ(CAS No.:545380-34-5)不仅通过调节上述离子通道在亨廷顿病(HD)研究中有效降低突变型亨廷顿蛋白水平,还在诱导多能干细胞(iPSCs)分化的神经元模型中表现出神经保护作用[14]。
Dehydroxymethylepoxyquinomicin (DHMEQ,AbMole,M11454)是一种基于微生物次级代谢产物Eepoxyquinomicin C的结构设计合成的特异性NF-κB抑制剂[18]。DHMEQ(CAS No.:287194-40-5)主要通过环氧基团与NF-κB组分中特定半胱氨酸残基的SH基团结合,从而阻断NF-κB的DNA结合能力,抑制其转录活性[18]。DHMEQ作为特异性的NF-κB抑制剂,在探究NF-κB与炎症/肿瘤的相关信号网络方面具有重要价值[19]。例如DHMEQ可增加前列腺癌细胞对放疗的敏感性[20],以及在胰岛组织的小鼠移植模型中降低组织损伤[21]。
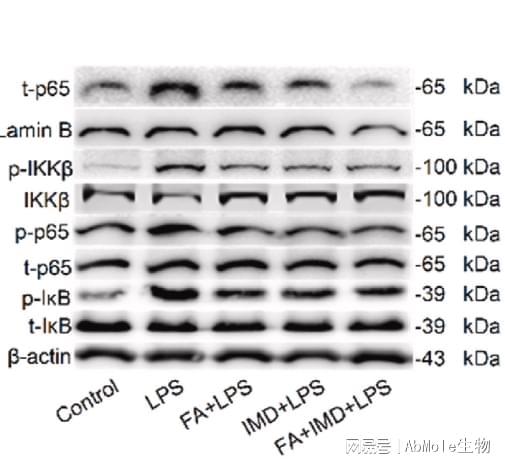
IMD-0354(AbMole,M2769)是一种小分子IKKβ抑制剂,通过选择性阻断IKKβ活性,有效抑制经典NF-κB信号通路的激活[22]。IMD-0354(IKK2 Inhibitor V)的应用广泛,覆盖炎症、肿瘤及代谢研究。在细胞模型中,IMD-0354能有效抑制多种肿瘤细胞(如肺癌细胞、黑色素瘤细胞)的增殖,并通过阻断NF-κB依赖的MET激活,增强细胞对凋亡的敏感性[23]。IMD-0354还在小鼠过敏性炎症模型表现出抗过敏和抗炎效果,其核心机制同样依赖于对NF-κB通路的抑制[24]。
Caffeic Acid Phenethyl Ester(CAPE,咖啡酸苯乙酯,AbMole,M2484)是一种从蜂胶中提取的生物活性多酚酯,具有广泛的科研应用价值。其作用机理主要涉及抗氧化、抗炎、抑制NF-κB信号通路等。CAPE可在微摩尔浓度下抑制NF-κB通路,降低炎症因子的表达,因此具有强大的抗炎活性。例如Caffeic Acid Phenethyl Ester(CAS No.:104594-70-9)在胶原抗体诱导的关节炎小鼠中以 1 mg/kg的剂量,能显著减轻关节炎症和骨破坏[25]。类似地,CAPE 在牙周炎大鼠模型中以10 μmol/kg/天的剂量腹腔注射 14 天,能降低血清炎症因子(IL-1β、TNF-α)的水平[26]。Caffeic Acid Phenethyl Ester还具有抗菌和抗肿瘤活性,例如有文献使用CAPE 并在1 nM至10 μM 浓度范围内测试其细胞活性,其中 10 μM的浓度显著抑制了骨肉瘤细胞增殖[27]。CAPE7(咖啡酸苯乙酯)对植物乳杆菌的最小抑菌浓度(MIC)为 125 μg/mL[28]。
Bay 11-7085(AbMole,M2435)是一种特异性核因子κB(NF-κB)抑制剂,通过靶向NF-κB信号通路发挥作用。Bay 11-7083(CAS No.:196309-76-9)可抑制IκBα磷酸化,阻断p65核转位,从而下调NF-κB的转录活性[29]。研究表明,Bay 11-7085不仅能直接抑制NF-κB,还能通过诱导PTEN表达间接降低AKT磷酸化[29]。在多种细胞模型中,如人骨肉瘤细胞(143B、MG63)、胃癌细胞(HGC27、MKN45)和神经胶质瘤细胞(U251),Bay 11-7085(BAY 11-7083)以剂量依赖性方式显著抑制细胞增殖、迁移和侵袭能力,同时促进凋亡[30, 31]。例如,在HGC27细胞中,其24小时半数抑制浓度(IC50)为24.88 nM[30]。此外,该化合物还能下调炎症相关蛋白(如NLRP3、IL-1β、IL-18)和上调凋亡标志物(如caspase 3、Bax)的表达[31]。
SN50(AbMole,南宫28M10545)是一种特异性抑制核因子κB(NF-κB)信号通路的肽类抑制剂,其核心作用机制是通过阻断NF-κB p65亚基的核转位,从而抑制下游炎症相关基因的激活[32]。也有研究表明,SN50能显著减少NF-κB p65在细胞核内的积累,同时降低胞质和核提取物中p65蛋白水平[33]。SN50(CAS No.:213546-53-3)同样具有抗炎能力,例如可有效抑制LPS(Lipopolysaccharides,脂多糖)诱导的小鼠肺损伤[34]。在大鼠模型中,SN50通过抑制NF-κB核转位,能减轻机械牵拉诱导的炎症反应,并降低内乳动脉中IL-6的生成[35]。
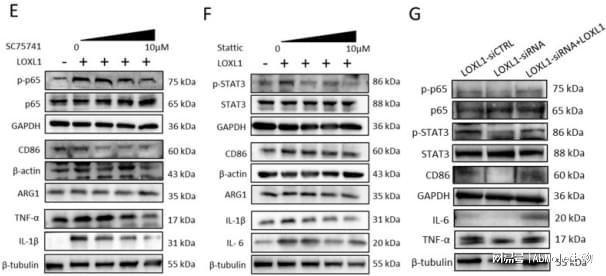
SC75741(AbMole,M4940)是一种特异性核因子κB(NF-κB)信号通路抑制剂,在多种细胞和动物模型中展现出广泛的科研应用价值。其作用机制主要通过直接抑制NF-κB的激活,从而调控下游炎症、免疫及细胞稳态相关通路。SC75741可以通过激活先天免疫,应对病毒复制和传播[36],例如保护小鼠(注射剂量为5 mg/kg/天)免受禽流感病毒的感染[37]。SC75741也具有抗肿瘤活性,可协同RIP2抑制剂GSK583抑制肿瘤干细胞[38]。
PDTC(吡咯烷二硫代氨基甲酸铵,AbMole,M4005)是一种特异性核因子κB(NF-κB)信号通路抑制剂,通过阻断IκB-α磷酸化和NF-κB p65核转位发挥功能。其生物学活性主要是抑制炎症因子(如TNF-α、IL-6、IL-1β)的表达。在细胞实验中,PDTC表现出多方面的调控作用。在GES-1胃黏膜细胞中,PDTC(2.5-60 μmol/L)可剂量依赖性地抑制壬基酚诱导的NF-κB/NLRP3通路激活,降低炎症因子释放[40]。Pyrrolidinedithiocarbamate ammonium(CAS No.:5108-96-3)在甲状腺癌细胞(BCPAP和PTC3-5)中,能抑制NF-κB蛋白表达,影响细胞增殖和迁移[41]。在动物模型中,PDTC(Ammonium pyrrolidinedithiocarbamate)对多种疾病模型具有改善作用:例如在DSS(Dextran sulfate sodium salt,葡聚糖硫酸钠,AbMole,M9443)诱导的溃疡性结肠炎小鼠中,PDTC通过抑制NF-κB活化,减少Th17细胞比例,降低促炎介质产生[42]。在慢性萎缩性胃炎(CAG)小鼠模型中,PDTC(100-200 mg/kg/day,灌胃8周)可减轻胃黏膜损伤[43]。
